|
Naturwissenschaften Radioaktiviät |
 |
Naturwissenschaften Weitere Informationen |
|
| Radiokarbonmethode zur Altersbestimmung |
| Emissionsverfälschte Altersmessungen |
 |
Radiokarbonmethode bleibt verlässliches Werkzeug, wenn sie durch 13C-Messungen ergänzt wird
Gute Nachrichten für Archäologen und Naturwissenschaftler! Sie werden auch künftig die Radiokarbonmethode als verlässliches Werkzeug für die Altersbestimmung von Artefakten und Probenmaterial verwenden können. Die durch den Kohlendioxidausstoss des Menschen vorangetriebene Abnahme des Kohlenstoffisotopes 14C in der Atmosphäre und die damit verbundene Verfälschung des Radiokarbonalters der Materialien lässt sich genau identifizieren - mit Hilfe einer Messung des Kohlenstoffisotopes 13C. Zu diesem Ergebnis kommt AWI-Geowissenschaftler Dr. Peter Köhler in einer Studie, die heute im Fachmagazin Environmental Research Letters erschienen ist.
 |
Wie lange noch können wir unsere beste Methode zur Altersbestimmung organischer Materialien einsetzen?
Diese Frage stellten sich Archäologen und Naturwissenschaftler vor etwa einem Jahr, als bekannt wurde, dass die Menschheit durch ihren Verbrauch fossiler Brennstoffe wie Kohle, Erdöl und Erdgas die Kohlenstoffisotopen-Bilanz der Erde derart verändert, dass die Radiokarbonmethode schon in wenigen Jahrzehnten ungenaue Altersangaben generieren wird. |
|
"Sollten die globalen Emissionen fossilen Kohlendioxids in naher Zukunft unverändert ansteigen wie im "business-as-usual"-Szenario des Weltklimarates prognostiziert, werden die Ergebnisse unserer Altersbestimmungen von neuem organischem Material im Jahr 2050 identisch sein mit jenen von rund 1'000 Jahre alten Proben. Im Jahr 2150 werden neue Proben dann in etwa so alt wie 3'000 Jahre alter Kohlenstoff erscheinen, im Extremfall sogar wie 4'300 Jahre altes Material. Das hiesse, frisches Probenmaterial, zum Beispiel von einem im nächsten Jahrhundert gefällten Baum, erscheint dann gemessen mit der Radiokarbonmethode genauso alt wie mehrere Jahrtausende altes Holz", erläutert Dr. Peter Köhler, Geowissenschaftler am Alfred-Wegener-Institut, Helmholtz-Zentrum für Polar- und Meeresforschung.
Er stellte sich im zurückliegenden Jahr die Frage, ob und wie sich diese verfälschte Alterung des Materials nachweisen liesse. Die Lösung hat er nun in einem weiteren Kohlenstoffisotop gefunden. "Wenn wir parallel zur Radiokarbonmethode auch den 13C-Wert der Probe bestimmen, können wir herausfinden, ob die Altersangabe vertrauenswürdig ist. Anhand des 13C-Wertes wird nämlich deutlich, ob der Kohlenstoff der Probe durch fossiles Kohlendioxid beeinflusst worden ist", sagt Peter Köhler.
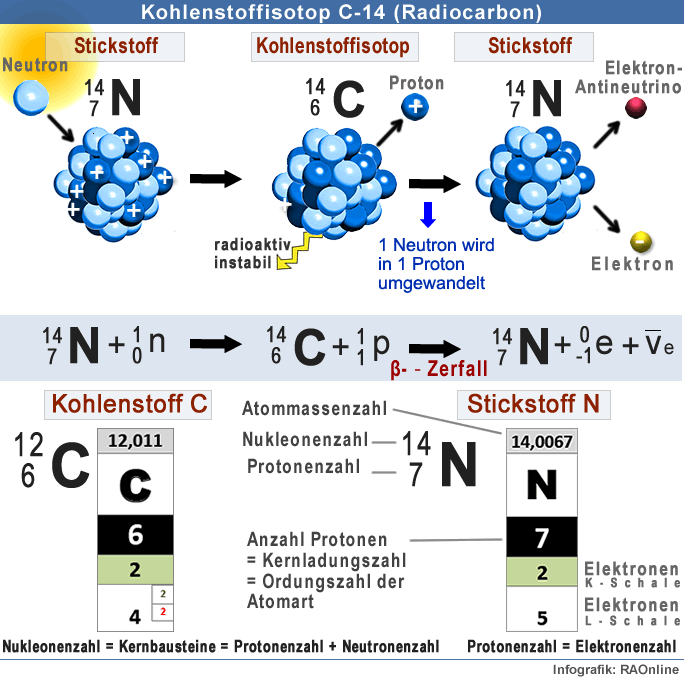
Kohlenstoff, den Lebewesen bei der Atmung, über die Photosynthese oder mit der Nahrung aufnehmen, enthält drei verschiedene Isotope: die beiden stabilen Isotope 12C und 13C sowie das radioaktive 14C. Letzteres wird durch Kernreaktionen in den oberen Schichten der Erdatmosphäre gebildet. Stirbt ein Tier oder eine Pflanze, zerfällt das in seinem Gewebe gebundene 14C mit einer konstanten Rate. Seine Halbwertzeit beträgt rund 6'000 Jahre.
Diesen Umstand machen sich Wissenschaftler bei der Altersbestimmung mithilfe der Radiokarbonmethode zunutze. Sie bestimmen dabei die Menge der verbliebenen 14C-Isotope in der Probe, setzen sie mit der Anzahl der 12C-Isotope in ein Verhältnis und vergleichen dieses wiederum mit einem vorher festgelegten Standard-Wert. "Wir stehen vor dem Problem, dass Erdgas, Erdöl und Kohle so alt sind, dass ihr Kohlenstoff keine 14C-Isotope mehr enthält. Verbrennen wir nun diese Rohstoffe, bringen wir grosse Mengen an 14C-freiem Kohlendioxid in die Atmosphäre. Die Folge ist, dass sich das Verhältnis von 14C zu 12C- ähnlich einem Alterungsprozess - verkleinert, zuerst in der Atmosphäre, später in allen mit ihr im Austausch stehenden Reservoiren. Dieses Phänomen kennen wir als den Suess-Effekt, benannt nach dem Physiker Hans E. Suess", sagt Peter Köhler.
Das 13C-Signal identifiziert den Unterschied
Diesen Suess-Effekt gibt es auch für das 13C-Isotop - eine Tatsache, die der AWI-Wissenschaftler zur Lösung des Datierungsproblems nutzte. "Durch das Verbrennen von Erdöl, Kohle und Erdgas verändert sich nicht nur das 14C-Signal in der Atmosphäre, sondern auch das stabile 13C-Signal. Das bedeutet: Habe ich in meiner Messung ein verändertes 13C-Signal, zeigt mir dieses an, dass auch die 14C-Altersangabe durch fossilen Kohlenstoff beeinflusst wurde. Liegt mein 13C-Signal dagegen innerhalb des zu erwartenden Bereiches, gibt es keinen Einfluss durch fossilen Kohlenstoff und die 14C-Altersangabe zeigt mir das korrekte Alter an", erläutert Peter Köhler.
In seiner Studie hatte der Wissenschaftler den 14C-Suess-Effekt und den 13C-Suess-Effekt bis zum Jahr 2500 mit dem Computermodell BICYCLE berechnet, welches den globalen Kohlenstoffkreislauf nachbildet. Seine Rechnungen basierten dabei auf den gängigen Emissionsszenarien des Weltklimarates. Anschliessend überprüfte er mithilfe weiterer Untersuchungen, ob seine Zukunftsprognosen auch dann standhielten, wenn es der Menschheit gelingen sollte, die Kohlendioxid-Konzentration in der Atmosphäre zu reduzieren.
In allen angenommenen Szenarien konnte die potentielle Verfälschung der Altersdatierung mit Hilfe des 13C-Suess-Effekts identifiziert werden. Lediglich in Regionen, die nur in langsamem Austausch mit der Atmosphäre stehen (z.B. der tiefe Pazifische Ozean), erscheint eine eindeutige Identifikation mithilfe des 13C-Suess-Effektes nicht möglich. Methodisch schwierig wird es auch, wenn die Menschheit in grossem Umfang beginnen sollte, Biomassen anzubauen, um Kohlendioxid zu binden, diese Biomasse dann verbrennt und das freiwerdende Kohlendioxid in unterirdischen Gesteinsschichten einlagert. Diese sogenannte BECCS-Methode wurde bereits in geringem Umfang in einigen Szenarien des Weltklimarates implementiert, ist aber nur eine von etlichen theoretisch möglichen Methoden, die Kohlendioxid-Konzentration in der Atmosphäre zu reduzieren.
Originalpublikation
Peter Koehler: Using the Suess effect on the stable carbon isotope to distinguish the future from the past in radiocarbon, Environ. Res. Lett. 11 124016. DOI: 10.1088/1748-9326/11/12/124016
 |
| Quelle: Text Alfred-Wegener-Institut, Dezember 2016 |
 |
 |
 |
 |
 |
| Isotop (gr: isos = gleich, topos = gleicher Ort) |
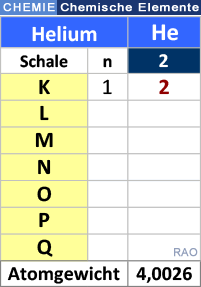
Als Isotope werden Atome bezeichnet, welche die gleiche Elektronen- und Protonenzahl haben, sich aber in der Anzahl ihre Neutronen unterscheiden. Diese Atome zeigen gleiche chemische Eigenschaften. Ihre Atommassenzahlen sind jedoch unterschiedlich. Isotope stehen daher an derselben Stelle im Periodensystem der Elemente.
Viele Elemente sind Mischungen verschiedener Isotopenarten (Bsp.: Kohlenstoff mit dem bekanntesten Isotop 14C, 14 = Nukleonenzahl (Kernbausteine) = annähernd Atommassenzahl). Diese Elemente sind als Mischelemente ein Isotopengemisch. Reinelemente wie Fluor, Natrium bestehen aus nur einer Atomart. Sie enthalten keine Isotope. |
| Lumineszenzdatierung |
| Bei Lumineszenzdatierungen werden Mineralien auf gespeichertes Licht untersucht und so datiert. |
| Petrefakt |
| Versteinerungen von Tieren und Pflanzen (= Fossilien) werden Petrefakte genannt. |
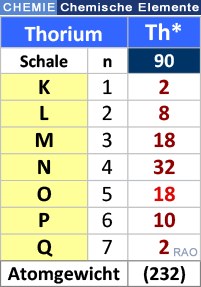
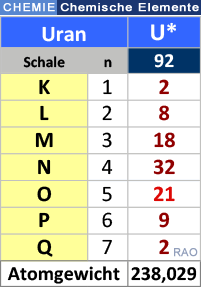
| Uran-Thorium-Methode |
| Die Uran-Thorium-Methode beruht darauf, dass Anteile von Uran und Thorium in den Proben mit den Anteilen zur Zeit der Entstehung der Petrefakte oder Gesteine ins Verhältnis gesetzt werden. Dabei werden die Halbwertszeiten des Zerfalls dieser beiden radioaktiven Metalle berücksichtigt (siehe auch: Radiokarbonmethode). |
|
 |
 |
 |
 |
|
| Jahrringe von Bäumen mit Fälldatum 2012 |
nach
oben
| Links |
 |
 |
 |
Externe Links |
|