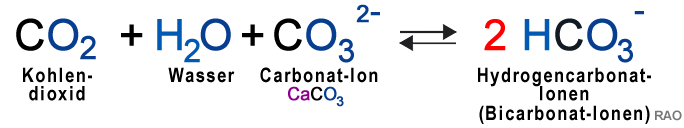| Informationen
über den Klimawandel |
 |
Klimawandel |
 |
Klimawandel Was ist das? - Treibhausgase |
 |
Klimawandel Weitere Informationen |
|
| Klimawandel:
Was ist das? - Kohlendioxid |
 |
| Die
wichtigsten Treibhausgase |
 |

|
Als Emission bezeichnet man jenen Teil der (Treibhaus-)Gase, welcher nach Abbau-, Umwandlungs- und Produktionsprozessen in die Atmosphäre gelangt ist.
Die Konzentration bezeichnet jenen Teil der Gase, welcher nach komplexen Interaktionsprozessen zwischen der Atmosphäre, der Biosphäre und den Ozeanen in der Atmosphäre verblieben ist. |
|
| Distickstoffmonoxid
(N2O) |
 |
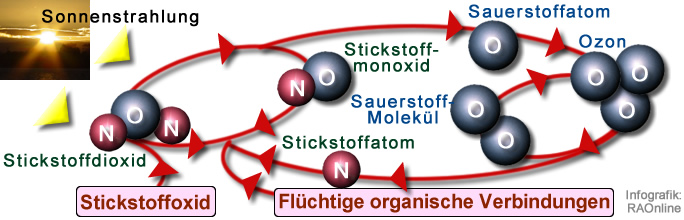
Distickstoffmonoxid (N2O) gehört wie Stickstoffmonoxid (NO) und Stickstoffdioxid (NO2) zu den Stickoxiden Stickoxide (NOx).
Stickoxide (NOx)sind an der photochemischen Bildung von Ozon beteiligt. Stickoxide sind als Vorläufersubstanzen auch an der Bildung von Ozon und sekundärem Feinstaub beteiligt. Sonnenlicht löst die Ozonbildung durch photolytische Spaltung von Stickstoffdioxid aus.
Stickoxid NO ist ein farb-, geruch- und geschmackloses Gas. In hoher Konzentration ist Stickstoffdioxid NO2 ist ein braunrotes, giftiges Gasmit einem starken und stechenden Geruch.
NOx entstehen in Verbrennungsprozessen (zum Beispiel bei Verbrennungsmotoren) bei hohen Temperaturen, die üblicherweise 5 bis 10 % NO2 enthalten. Bei Dieselmotoren werden nach der Abgasbehandlung bis zu 70 %NO2-Anteil gemessen. Im Kontakt mit den oxydierenden Stoffen wie Sauerstoff O2 oder Ozon O3 in der Umgebungsluft verwandelt sich NO rasch zu NO2. Zu den NOx-Quellen gehören Privathaushalte, Kraftfahrzeuge sowie Industrieanlagen.
Das Stickstoffdioxid NO2 hat schädliche Auswirkungen auf den Menschen. Es ruft Atembeschwerden und Schleimhautreizungen hervor. Es kann akute Bronchitis, Husten und Herz-Kreislauf-Beschwerden
verschlimmern.
Zur Bestimmung der Luftqualität werden in der Schweiz die Konzentrationen von Feinstaub, Stickstoffdioxid und Ozon regelmässig gemessen.
60 % des N2O-Ausstosses stammt aus natürlichen Quellen und 40% aus menschlichen Aktivitäten wie dem Gebrauch von Dünger für die Landwirtschaft, dem Verbrennen von Biomasse, der Bodenbearbeitung usw.
Die Auswirkungen des N2O-Anstiegs in den letzten 100 Jahren ist 298mal stärker als diejenigen einer gleiche Menge CO2.
Das Distickstoffmonoxid spielt auch eine wichtige Rolle bei Zerstören der Ozonschicht in der Stratosphäre. Die Ozonschicht schützt den Menschen vor den schädliche UV-Strahlen.
Die
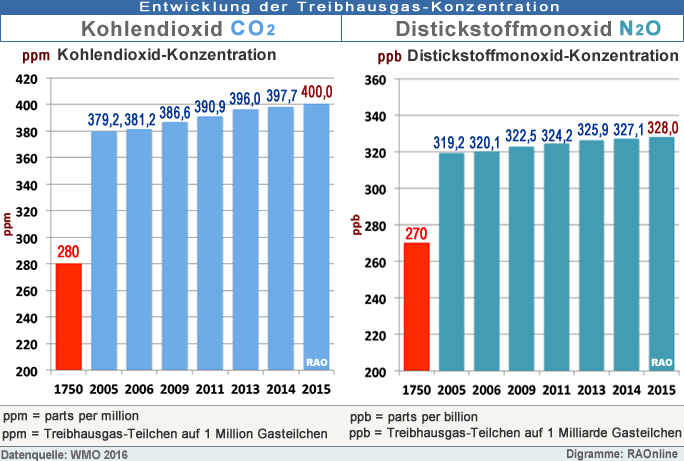
Distickstoffmonoxid (N2O)-Konzentration
war 2006 mit 320,1 ppm (= parts per million = Teile pro eine Million) um 0,25 Prozent höher als 2005 mit 319,2 ppm.
Dies ist ebenfalls ein Rekordwert. Distickstoffmonoxid wird auch als "Lachgas" bezeichnet.
Lachgas (Distickstoffmonoxid N2O) trägt mit 6,24% zur globalen Strahlungsbilanz bei. Es wird aus natürlichen und anthropogenen (von Menschen verursachten) Quellen, einschliesslich der Meere, Verbrennung von Biomasse, die Verwendung von Düngemitteln und verschiedenen industriellen Prozessen, in die Atmosphäre abgegeben.
Fast
ein Drittel der Stickstoffdioxid-Menge, welche an die Luft abgegeben wird,
ist auf Tätigkeiten der Menschen wie ...
 das
Verbrennen von fossilen Brennstoffen, das
Verbrennen von fossilen Brennstoffen,
 das Verbrennen von Biomassen, das Verbrennen von Biomassen,
 den Gebrauch von Düngemitteln den Gebrauch von Düngemitteln
 und gewissen industriellen Prozessen und gewissen industriellen Prozessen
zurückzuführen.
Distickstoffmonoxid (N2O) wird u.a. von Dieselfahrzeugen, welche noch nicht mit der neusten Technologie ausgerüstet sind, ausgestossen. Distickstoffmonoxid (N2O) greift die Atemwege der Menschen an.
nach
oben
| Methan-Gas
(CH4) |
 |
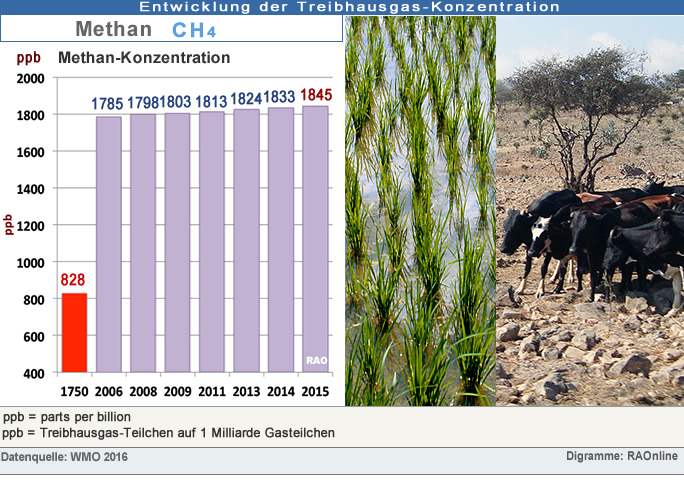
Vor Beginn des industriellen Zeitalters in der Mitte des 18. Jahrhunderts betrug die atmosphärische Methangas-Konzentration ca. 700 ppb (= parts per billion = Teile pro eine Milliarde). Seit 1750 ist die atmosphärische Methangas-Konzentration um 158% gestiegen. Die Hauptverursacher von Methangas sind menschlichen Aktivitäten wie Viehzucht, Reisanbau, Ausbeutung fossiler Brennstoffe und Deponien.
Methan ist das zweitwichtigste langlebige Treibhausgas. Ungefähr 40% des Methans, welche in die Atmosphäre entweicht, stammt aus natürlichen Quellen wie Feuchtlandgebieten oder Termiten. Ungefähr 60% des Methanausstosses rührt von menschlichen Aktivitäten wie der Weidewirtschaft mit Vieh, der Viehzucht, dem Reisanbau, dem Verbrennen von Biomasse, der Ausbeutung von fossilen Energieträgern usw.
Rund
60 Prozent der Methangas-Menge, welche an die Luft abgegeben wird, ist
auf Tätigkeiten der Menschen wie ...
 die
Gewinnung von fossilen Brennstoffen, die
Gewinnung von fossilen Brennstoffen,
 das Verbrennen von Biomassen, das Verbrennen von Biomassen,
 den Reisanbau, den Reisanbau,
 die Herdenhaltung von Gross- und Kleinvieh die Herdenhaltung von Gross- und Kleinvieh
... zurückzuführen.
Rund
60 Prozent der Methangas-Menge stammt aus den natürlichen Umwandlungsprozessen
in Feuchtgebieten und die Tätigkeiten von Termiten.
Sumpfgase:
In Torfmooren und sehr lange bestehenden Sümpfen ist eine grosse Menge an Kohlendioxid
(CO2) in den unter dem Wasser liegenden Pflanzenteilen gespeichert. Das Kohlendioxid (CO2) wird frei und gelangt in die Atmosphäre, wenn das Moor oder der Sumpf trockengelegt wird. Bei einer Renaturierung dieser Moore oder Sümpfe wird das neu herangewachsene Pflanzenmaterial wieder unter Wasser gesetzt. Beim Vermodern dieser Pflanzen entsteht eine riesige Menge an Methan-Gas (CH4) , welches die Atmosphäre zusätzlich mit Treihausgasen belastet.
nach
oben
| Kohlendioxid (CO2) |
 |
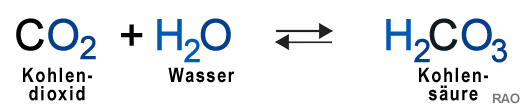
Das CO2 ist jenes Treibhausgas, welches am häufigsten durch menschliche Aktivitäten in die Atmosphäre abgegeben wird. Es ist zu 85% am Treibhauseffekt auf dieser Erde beteiligt.
Die Kohlendioxid
(CO2)-Konzentration
ist seit der Mitte des 18. Jahrhunderts um rund 40 Prozent angestiegen. In der vorindustriellen Zeit vor 1750 betrug die CO2-Konzentration noch 280 ppm.
In der Zeit vor 1750 war der CO2-Austausch zwischen der Atmosphäre, der Biosphäre und den Weltmeeren in einem Gleichgewicht.
 Kohlendioxid
wird hauptsächlich beim Verbrennen von fossilen Brennstoffen wie Heizöl,
Benzin, Diesel usw. erzeugt. Kohlendioxid
wird hauptsächlich beim Verbrennen von fossilen Brennstoffen wie Heizöl,
Benzin, Diesel usw. erzeugt.
 |
| Berichte über Kohlenstoffverbindungen |
|
Sumpfgase:
In Torfmooren und sehr lange bestehenden Sümpfen ist eine grosse Menge an Kohlendioxid
(CO2) in den unter dem Wasser liegenden Pflanzenteilen gespeichert. Das Kohlendioxid (CO2) wird frei und gelangt in die Atmosphäre, wenn das Moor oder der Sumpf trockengelegt wird.
In den arktischen Permfrostgebieten schmilzt als Folge der globalen Klimaerwärmung grosse Menge des beständigen Eiskörpers im Boden, dem Permafrost. Ausgedehnte Sumpflächen entstehen. Aus diesen neu entstandenen Sümpfen entweichen Kohlendioxid-Gase.
Bei einer Renaturierung dieser Moore oder Sümpfe wird das neu herangewachsene Pflanzenmaterial wieder unter Wasser gesetzt. Beim Vermodern dieser Pflanzen entsteht eine riesige Menge an Methan-Gas (CH4) , welches die Atmosphäre zusätzlich mit Treihausgasen belastet.
 |
Quelle:
World Meteorological Organization WMO, 2007 und 2012
Text: RAOnline |
nach
oben
| Weitere Treibhausgase |
 |
Schwefelhexafluorid (SF6)
Schwefelhexafluorid, kurz SF6, spielt als Isoliergas in elektrischen Schaltgeräten der verschiedenen Spannungsebenen eine wichtige Rolle beim Unterbrechen und Umleiten von Stromflüssen. Gleichzeitig ist es eines der wirksamsten Treibhausgase mit einer sehr langen Lebensdauer und obwohl augenblicklich die Konzentration von SF6 in der Atmosphäre noch sehr gering ist, steigt sie über die Jahre beständig an. (Textquelle: Fraunhofer IEE 2019)
SF6 kommt vor allem bei Geräten im Spannungsbereich von mehr als 1'000 Volt zum Einsatz. Aufgrund seiner physikalischen Eigenschaften dient es als Isolier- und Löschgas. Es ist farb- und geruchlos, ungiftig und brennt nicht.
Grosse Mengen des SF6-Gases werden in der Elektroindustrie und im Apparatebau eingesetzt, ebensobei der Herstellung von Glasfasern für die Nachrichten- und Informationsübertragungstechnik wie auch in der Halbleiterindustrie.
SF6 ist in Schaltanlagen und -geräten, in Messwandlern, gasisolierten Leitungen, Hochspannungsdurchfü̈hrungen und Kondensatoren zu finden. Das Gas ist auch in den elektrischen Schaltanlagen bei Wandkraftanlagen verbaut und wird meistens in geschlossenen Systemen verwendet. Bei korrekter Verwendung und Entsorgung entstehen hier keine klimaschädlichen Einflüsse. (Informationsquelle: Wissenschaftliche Dienste des Deutschen Bundestages, Sachstand Schwefelhexafluorid, Oktober 2022)
| Wichtige
Begriffe |
 |
nach
oben
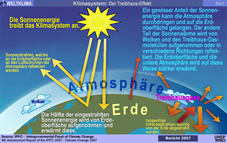
| Erde:
Treibhaus-Effekt |
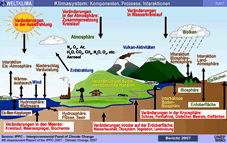
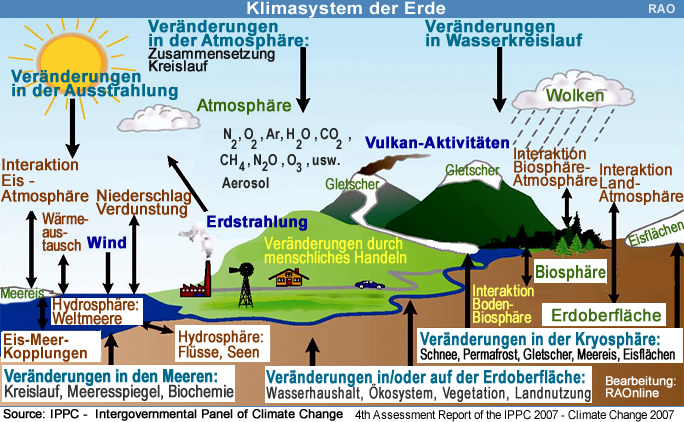
Erde:
Klimasystem Erde |
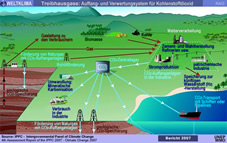
Kohlendioxid - Management |
 |
 |
 |
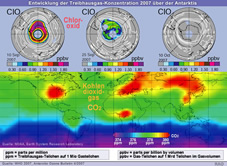
| Treibhausgase 2007 |
Treibhausgase 2007 |
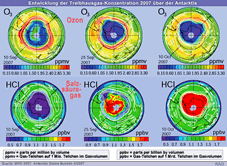
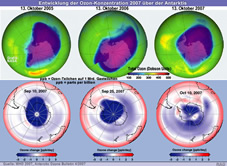
Ozon-Konzentration 2007 |
 |
 |
 |
nach
oben
| Stichworte: |
Albedo,
Aerosol, Abstrahlung, Atmosphäre, Auffanganlage, Bergbau, Biomasse,
Biosphäre, Distickstoffoxid, Eis, Energie, Erde, Erdstrahlung, Herstellung,
Hydrosphäre, Industrie, Interaktion, Karbonisation, Kohlendioxid ,
Kreislauf, Kryosphäre, Gletscher, Lagerung, Naturgas, Meer, Methan,
Niederschlag, Pipeline, Produktion, Reflexion, Speicherung, Strahlungsbilanz,
Stromproduktion, Strahlungsenergie, Transport, Treibhaus-Gas, Schnee, Sonnenstrahlung,
Verdunstung, Vulkan, Wärme, Wind, Wolke, Kohlendioxid -Management
und - verarbeitung, Treibhaus-Effekt, Umwandlung, Verbraucher, Verarbeitung,
Wasserstoff |
|



![]() das
Verbrennen von fossilen Brennstoffen,
das
Verbrennen von fossilen Brennstoffen, ![]() das Verbrennen von Biomassen,
das Verbrennen von Biomassen, ![]() den Gebrauch von Düngemitteln
den Gebrauch von Düngemitteln ![]() und gewissen industriellen Prozessen
und gewissen industriellen Prozessen 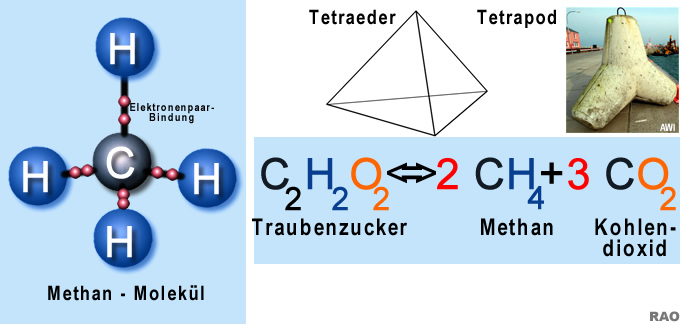
![]() die
Gewinnung von fossilen Brennstoffen,
die
Gewinnung von fossilen Brennstoffen, ![]() das Verbrennen von Biomassen,
das Verbrennen von Biomassen, ![]() den Reisanbau,
den Reisanbau, ![]() die Herdenhaltung von Gross- und Kleinvieh
die Herdenhaltung von Gross- und Kleinvieh 
![]() Kohlendioxid
wird hauptsächlich beim Verbrennen von fossilen Brennstoffen wie Heizöl,
Benzin, Diesel usw. erzeugt.
Kohlendioxid
wird hauptsächlich beim Verbrennen von fossilen Brennstoffen wie Heizöl,
Benzin, Diesel usw. erzeugt.